Si buscas
hosting web,
dominios web,
correos empresariales o
crear páginas web gratis,
ingresa a
PaginaMX
Por otro lado, si buscas crear códigos qr online ingresa al Creador de Códigos QR más potente que existe




Combustion from Possible Metrics on Vimeo.
Se denomina reacción de reducción-oxidación, óxido-reducción, o simplemente reacción redox, a toda reacción química en la cual existe una transferencia electrónica entre los reactivos, dando lugar a un cambio en los estados de oxidación de los mismos con respecto a los productos.
Para que exista una reacción redox, en el sistema debe haber un elemento que ceda electrones y otro que los acepte:
El agente reductor es aquel elemento químico que suministra electrones de su estructura química al medio, aumentando su estado de oxidación, es decir, siendo oxidado.
El agente oxidante es el elemento químico que tiende a captar esos electrones, quedando con un estado de oxidación inferior al que tenía, es decir, siendo reducido.1
Cuando un elemento químico reductor cede electrones al medio se convierte en un elemento oxidado, y la relación que guarda con su precursor queda establecida mediante lo que se llama un par redox. Análogamente, se dice que cuando un elemento químico capta electrones del medio se convierte en un elemento reducido, e igualmente forma un par redox con su precursor oxidado.
COMBUSTIÓN
La combustión es una reacción química en la cual generalmente se desprende una gran cantidad de calor y luz.
En toda combustión existe un elemento que arde (combustible) y otro que produce la combustión (comburente), generalmente oxígeno en forma de O2 gaseoso. Los explosivos tienen oxígeno ligado químicamente por lo que no necesitan el oxígeno del aire para realizar la combustión.
Los tipos más frecuentes de combustible son los materiales orgánicos que contienen carbono e hidrógeno. En una reacción completa todos los elementos tienen el mayor estado de oxidación. Los productos que se forman son el dióxido de carbono (CO2) y el agua, el dióxido de azufre (SO2) (si el combustible contiene azufre) y pueden aparecer óxidos de nitrógeno (NOx), dependiendo de la temperatura y la cantidad de oxígeno en la reacción.
En la combustión incompleta los productos que se queman pueden no reaccionar con el mayor estado de oxidación, debido a que el comburente y el combustible no están en la proporción adecuada, dando como resultado compuestos como el monóxido de carbono (CO). Además, pueden generarse cenizas.
El proceso de destruir materiales por combustión se conoce como incineración.
Para iniciar la combustión de cualquier combustible, es necesario alcanzar una temperatura mínima, llamada temperatura de ignición, que se define como, en °C y a 1 atm, temperatura a la que los vapores de un combustible arden espontáneamente.
http://www.youtube.com/watch?feature=endscreen&NR=1&v=p7fHMmiNy0g
Rubric: Chemical Poster Project
Combustion from Renaud Hallée on Vimeo.
Intoxicación por monóxido de carbono
La causa más frecuente de defunciones asociadas a la temporada invernal ha sido la intoxicación por monóxido de carbono con 45 por ciento , seguido de la hipotermia con 36 por ciento y las quemaduras con 19 por ciento , según datos de la Secretaría de Salud.
Los grupos de edad afectados en esta temporada invernal han sido de 25 a 44 años con 34 por ciento ; los mayores de 65 años con 22 por ciento ; de 45 a 64 años con 19 por ciento ; de 1 a 4 años con 13 por ciento y los menores de un año y de 15 a 24 años con 6 por ciento .

Reactividad de X2 F2 > CI2 > Br2 ( > I2)
La combustión es una oxidación, habrán de intervenir, para que ésta se produzca, un material que se oxide, al que llamaremos COMBUSTIBLE, y un elemento oxidante, que llamaremos COMBURENTE. Para que la reacción de oxidación comience, habrá que disponer, además, de una cierta cantidad de energía, que llamaremos ENERGIA DE ACTIVACION (habitualmente CALOR).
Sin la presencia simultánea de estos tres elementos no es posible obtener fuego.
1.1. COMBUSTIBLE. COMBURENTE. ENERGIA DE ACTIVACION
1.1.1. COMBUSTIBLE
Sustancia que en presencia de oxígeno y aportándole una cierta energía de activación, es capaz de arder. Los combustibles pueden clasificarse, según su naturaleza:
¨ Combustibles sólidos: Carbón mineral (Antracita, carbón de coque, etc.), madera, plástico, textiles, etc.
¨ Combustibles líquidos: Productos de destilación del petróleo (gasolina, gas-oil, fuel-oil, aceites, etc.), alcoholes, disolventes, etc.
¨ Combustibles gaseosos: Gas natural, gas ciudad, metano, propano, butano, etileno, hidrógeno, etc.
1.1.2. COMBURENTE
Sustancia en cuya presencia el combustible puede arder. De forma general, se considera al oxígeno como el comburente típico. Se encuentra en el aire en una concentración del 21% en volumen.
Existen otros, tales como el ácido perclórico, el ozono, el peróxido de hidrógeno, etc.
Los combustibles que presentan un alto número de átomos de oxígeno en su molécula no necesitan comburente para arder (peróxidos orgánicos).
1.1.3. ENERGIA DE ACTIVACION
Es la energía necesaria para que la reacción se inicie.
Las fuentes de ignición que proporcionan esta energía pueden ser: sobrecargas o cortocircuitos eléctricos, rozamientos entre partes metálicas, equipos de soldadura, estufas, reacciones químicas, chispas, etc.
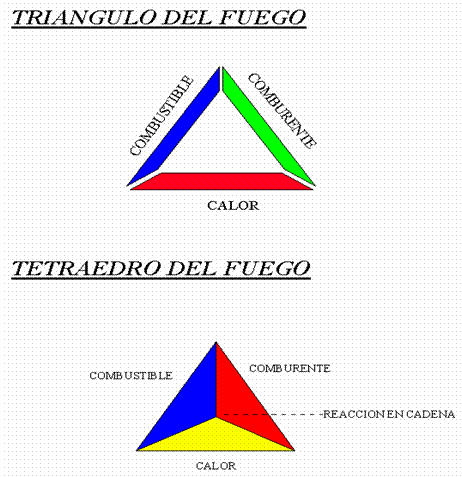
TRIANGULO Y TETRAEDRO DEL FUEGO
El fuego no puede existir sin la conjunción simultánea del Combustible (material que arde), comburente (oxígeno del aire) y de la energía de activación (chispas mecánicas, soldaduras, fallos eléctricos, etc.).
Si falta alguno de estos elementos, la combustión no es posible. A cada uno de estos elementos se los representa como lados de un triángulo, llamado TRIANGULO DEL FUEGO, que es la representación de una combustión sin llama o incandescente.
Existe otro factor, "reacción en cadena", que interviene de manera decisiva en el incendio. Si se interrumpe la transmisión de calor de unas partículas a otras del combustible, no será posible la continuación del incendio, por lo que ampliando el concepto de Triángulo del Fuego a otro similar con cuatro factores obtendremos el TETRAEDRO DEL FUEGO, que representa una combustión con llama.
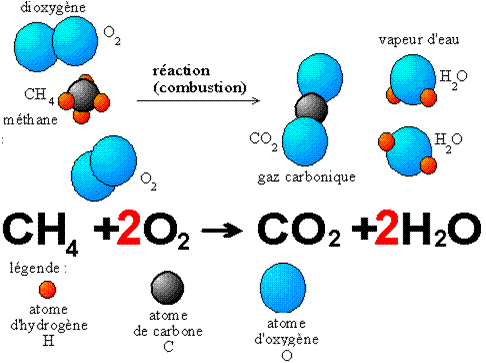
![]()
![]()
![]()
![]()
![]()
![]()